iPS細胞、2製品を承認=心疾患とパーキンソン病治療―世界初の実用化・厚労省
厚生労働省は6日、世界初となる人工多能性幹細胞(iPS細胞)を使った二つの再生医療製品について、条件付きで製造販売を承認したと発表した。iPS細胞を使った医療製品の承認は世界初。今後、企業からの申請を経て公的医療保険の対象となり、保険診療で使えるようになる見通し。
承認されたのは、大阪大発のベンチャー企業「クオリプス」(東京)による心臓病患者向け心筋細胞シート「リハート」と、住友ファーマ(大阪)のパーキンソン病患者向けドーパミン神経細胞「アムシェプリ」。いずれも今後7年かけて有効性などのデータを追加収集。リハートは75人、アムシェプリは35人を目標に患者の治療実績を調査し、本承認の可否を改めて審査する。
2月に同省の専門部会が「条件・期限付き承認制度」で了承していた。上野賢一郎厚労相は6日の閣議後記者会見で「世界中の患者の救いになることを願っている」と話した。
リハートは、iPS細胞から作った心筋細胞を直径4~5センチ、厚さ約0.1ミリのシート状に加工し、患者の心臓に貼り付けて機能を回復させる。アムシェプリは神経細胞500万~1000万個を脳の中央部に移植し、運動機能の改善を図る。
【時事通信社】
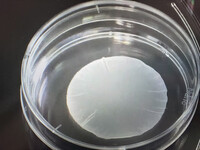
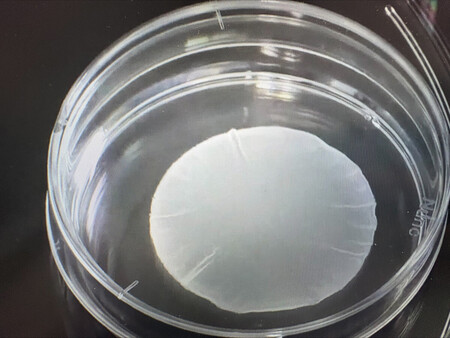
〔写真説明〕大阪大発のベンチャー企業「クオリプス」がiPS細胞から作製した心筋シート(同社提供)
〔写真説明〕住友ファーマが培養したiPS細胞(同社提供)
〔写真説明〕厚生労働省=東京都千代田区
2026年03月06日 13時13分