iPS細胞由来製品を承認へ=心疾患とパーキンソン病治療―世界初の実用化・厚労省部会
厚生労働省の専門部会は19日、人工多能性幹細胞(iPS細胞)を使った二つの再生医療製品について、製造販売承認をいずれも了承した。近く厚労相が正式承認し、世界初のiPS細胞由来の医療製品となる。
審査するのは、大阪大発のベンチャー企業「クオリプス」(東京都中央区)による心臓病患者向け心筋細胞シート「リハート(商品名)」と、住友ファーマ(大阪市)のパーキンソン病患者向けドーパミン神経細胞「アムシェプリ(商品名)」。いずれも、進行すると従来の治療では症状の改善が難しくなる重い疾患だ。
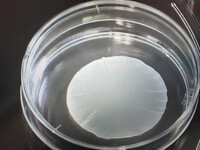
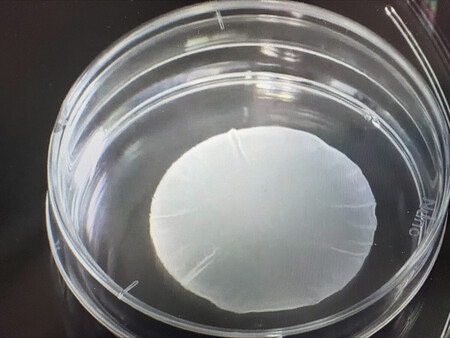
心筋シートは、虚血性心筋症による心不全患者を対象に、阪大の研究チームが2020年に世界で初めて移植手術を実施。直径4~5センチ、厚さ約0.1ミリのシートを心臓表面に貼り付けて、弱った心臓の機能を回復させる。23年までに計8人で臨床試験(治験)を行い、安全性や症状改善が確認されたとしている。
ドーパミン神経細胞は、京都大付属病院などが18~23年、50~60代の患者で治験を実施。500万~1000万個を脳の中央部に移植し、2年間経過観察を続けたところ、患者6人中4人で運動機能の改善が確認された。重篤な副作用はなく、若く症状の軽い患者ほど効果が高い傾向がみられたという。
iPS細胞は、患者本人や他人の細胞から作製でき、拒絶反応の低減や安定供給が期待される一方、長期的な安全性などが課題とされてきた。
いずれも、有効性が「推定」の段階でも一定の期限や条件の下で承認できる「条件・期限付き承認制度」で審査された。承認後も最長7年をかけて有効性などのデータを追加収集し、本承認するかを専門部会が判断する。
〔写真説明〕大阪大発のベンチャー企業「クオリプス」がiPS細胞から作製した心筋シート(同社提供)
〔写真説明〕iPS細胞を使った再生医療製品について審議する厚生労働省の専門部会=19日午後、東京都千代田区
〔写真説明〕住友ファーマで培養したiPS細胞(同社提供)
2026年02月20日 12時31分